
Лекарство от ВИЧ. Как ученые из России и США вплотную подошли к решению проблемы «чумы ХХ века»
Эпидемия вируса иммунодефицита человека, атакующего защитную систему организма, началась в 1980-е годы, но медики до сих пор не могут остановить ее распространение. ВИЧ быстро приобретает устойчивость к препаратам и становится невосприимчив к лечению. Как подавить размножение вируса в организме, какой новый препарат, способный полностью излечить пациентов, сейчас разрабатывают российские ученые и можно ли создать эффективную вакцину против ВИЧ — читайте в материале «Сноба»

Заражен каждый сотый
В России на 2022 год количество инфицированных ВИЧ достигло около 1,5 миллиона человек, что составляет 1% населения страны — такие данные приводит доктор медицинских наук Вадим Покровский, руководитель специализированного научно-исследовательского отдела эпидемиологии и профилактики СПИД ЦНИИ эпидемиологии Роспотребнадзора. По прогнозам эксперта, до 2030 года можно ожидать еще 660 тыс. новых случаев инфекции.
Антиретровирусная терапия сегодня помогает пациентам вести нормальную жизнь и снижает риск заражения других людей даже при обмене биологическими жидкостями (к которому относятся не только незащищенные половые контакты, но и роды и грудное вскармливание). Но терапия не может излечить человека полностью, чтобы его организм стал свободен от вируса. Сегодня известно всего о трех случаях выздоровления от этой инфекции. «Берлинскому пациенту» Тимоти Рэю Брауну в 2007 году из-за лейкоза провели трансплантацию костного мозга. У донора была мутация в гене CCR5, которая делает клетки крови устойчивыми к вирусу. В результате Браун перестал принимать антиретровирусные препараты и прожил больше 12 лет без симптомов ВИЧ. Вирус не обнаруживался в крови Брауна, но в 2020 году он все-таки умер от лейкоза. «Лондонский пациент» Адам Кастильехо и «дюссельдорфский пациент», имя которого ученые не разглашали, излечились тем же путем. Однако трансплантация костного мозга — серьезная операция, которую слишком опасно было бы делать всем пациентам с ВИЧ. К тому же, пока медики не могут позволить себе тратить на это донорский костный мозг, который очень сложно найти.
Поэтому исследователи продолжают активный поиск новых лекарств. В новой работе российские ученые из ФИЦ биотехнологии РАН в сотрудничестве с коллегами из США и Италии предприняли успешную попытку получить прототип лекарственного средства, которое было бы способно убивать вирус иммунодефицита человека в его «логове», в нейронах. Таким образом, объединенная международная команда впервые приблизилась к получению лекарства для излечения ВИЧ, а не перевода болезни в хроническую форму.
Для этого они смоделировали, синтезировали, оптимизировали и детально исследовали биологическую активность более 250 оригинальных соединений, производных N-фенил-1-(фенилсульфонил)-1H-1,2,4-триазол-3-аминов. Первоначальная идея состояла в том, чтобы создать новое поколение лекарств — ингибиторов обратной транскриптазы ВИЧ (фермента, отвечающего за «размножение» вируса), при этом такие препараты должны успешно проходить через гематоэнцефалический барьер, проникать в нейроны, уничтожать там вирус и быть не токсичным для самих нервных клеток. Последнее, как рассказали нам исследователи, оказалось самым трудным: нужно было создать препарат, достаточно эффективный в такой концентрации, которая не вредит клеткам организма-«хозяина».
Чтобы понять механизм работы лекарств этого класса, кратко поясним, как самовоспроизводятся вирусы. РНК-вирусам, в том числе ВИЧ, необходимо перевести свою наследственную информацию из РНК в ДНК. Это нужно, чтобы заставить клетку синтезировать новые частицы вируса, ведь вирусы не могут размножаться без использования наследственного механизма клеток хозяина. Для подавления работы вирусного фермента ученые предложили новое поколение ненуклеозидных ингибиторов обратной транскриптазы ВИЧ, блокирующих собой активный центр фермента вируса. Изобретенные молекулы мешают ферменту менять форму, что необходимо для его нормальной работы. В итоге вирус не может тиражировать свои копии, которые могли бы заражать новые клетки. О результатах своей работы ученые рассказали в ведущем мировом журнале в области разработки новых лекарственных средств Journal of Medicinal Chemistry.

Блеск и нищета антиретровирусной терапии
У существующих препаратов от ВИЧ немало недостатков. Во-первых, вирус быстро мутирует и вырабатывает резистентность: от 7 до 20% пациентов (в зависимости от региона проживания) устойчивы к терапии с самого начала, а при возобновлении лечения препарат может быть неэффективным для 40% больных. Во-вторых, существующие препараты противопоказаны некоторым пациентам по состоянию здоровья. В-третьих, современные лекарства из-за более высокой стоимости доступны не во всех странах, а более дешевые препараты предыдущего поколения достаточно токсичны и могут вызвать цирроз печени, панкреатит и другие тяжелые последствия, а со временем — и тяжелые поражения нейронов головного мозга. Чтобы компенсировать развитие резистентности, антиретровирусные препараты от ВИЧ чаще всего назначают в комбинациях. В итоге пациент в лучшем случае принимает комбинацию лекарств много лет подряд, но не может избавиться от вируса полностью. Кроме того, терапия пока не позволяет победить неврологические осложнения при ВИЧ-инфекции — от небольших нарушений памяти до тяжелых симптомов, похожих на деменцию. Все эти проблемы стараются решить российские и американские ученые.
«Эти исследования совместно с американскими коллегами мы ведем с 2016 года. С нашей стороны работы частично финансировал Российский фонд фундаментальных исследований, который в прошлом году преобразовали в Российский центр научной информации, также значительные инвестиции были сделаны непосредственно ФИЦ биотехнологии РАН, а американские исследования были профинансированы рядом грантов Национального института здоровья США. Уникальность новой молекулы в том, что она проникает сквозь гематоэнцефалический барьер, то есть находит вирус в нейронах мозга, где он может дремать долгое время, прячась от других лекарств. Так как соединение проникает через этот барьер, оно сможет еще и помочь в борьбе с ВИЧ-индуцированными неврологическими расстройствами», — комментирует ведущий автор работы, академик Вадим Макаров, доктор фармацевтических наук и глава лаборатории биомедицинской химии ФИЦ биотехнологии РАН.
Чтобы достичь такого результата, российские ученые предложили идею, разработали дизайн и пути синтеза сотен соединений-кандидатов нового класса, которые, с одной стороны, обладают способностью блокировать обратную транскриптазу ВИЧ и, с другой стороны, проходят гематоэнцефалический барьер. Отечественные химики и биологи получили целевые соединения, исследовали их токсичность и фармакокинетику, определили концентрацию соединений не только в крови, но в мозге животных, проследили «судьбу» и превращения молекул, когда они попадают в организм. Американские и итальянские соавторы занимались исследованием эффективности и безопасности соединений-лидеров для нейронов. В итоге исследователи получили кандидата на лекарственное средство, которое будет успешно подавлять воспроизводство вируса иммунодефицита человека даже при очень низких, пикомолярных концентрациях. Это делает его потенциальным препаратом с минимально возможным набором побочных эффектов. Эксперименты показали, что прототип проявляет высокую активность как против «дикого» мутантного типа ВИЧ A17 (K103N/Y181C), так и против других штаммов вируса, которые чаще всего устойчивы к действию уже одобренных лекарств. При этом он безопасен для нейронов.
Можно ли создать вакцину от ВИЧ?
Пока что терапия развивается медленно, а как насчет предотвращения заражения? Создать прививку очень сложно: «убитые» вирусы не могут натренировать иммунитет нужным образом, ВИЧ долго может быть в латентном виде и прятаться от иммунитета, да и оболочка у него намного более изменчива, чем у большинства других вирусов. Кроме того, для испытаний этой вакцины сложно найти добровольцев, а ее действие на обезьян и на людей может сильно отличаться. Однако попытки создать такую прививку продолжаются. В США в прошлом году прошла проверку безопасности вакцина на основе видоизмененного аденовируса AAV8. В Таиланде экспериментальная вакцина RV144 оказалась безопасной и снизила риски заражения на 31%, что стало большим успехом для науки. Правда, для одобрения местным министерством здравоохранения нужна эффективность не менее 50%, так что пока применять такой результат нельзя.
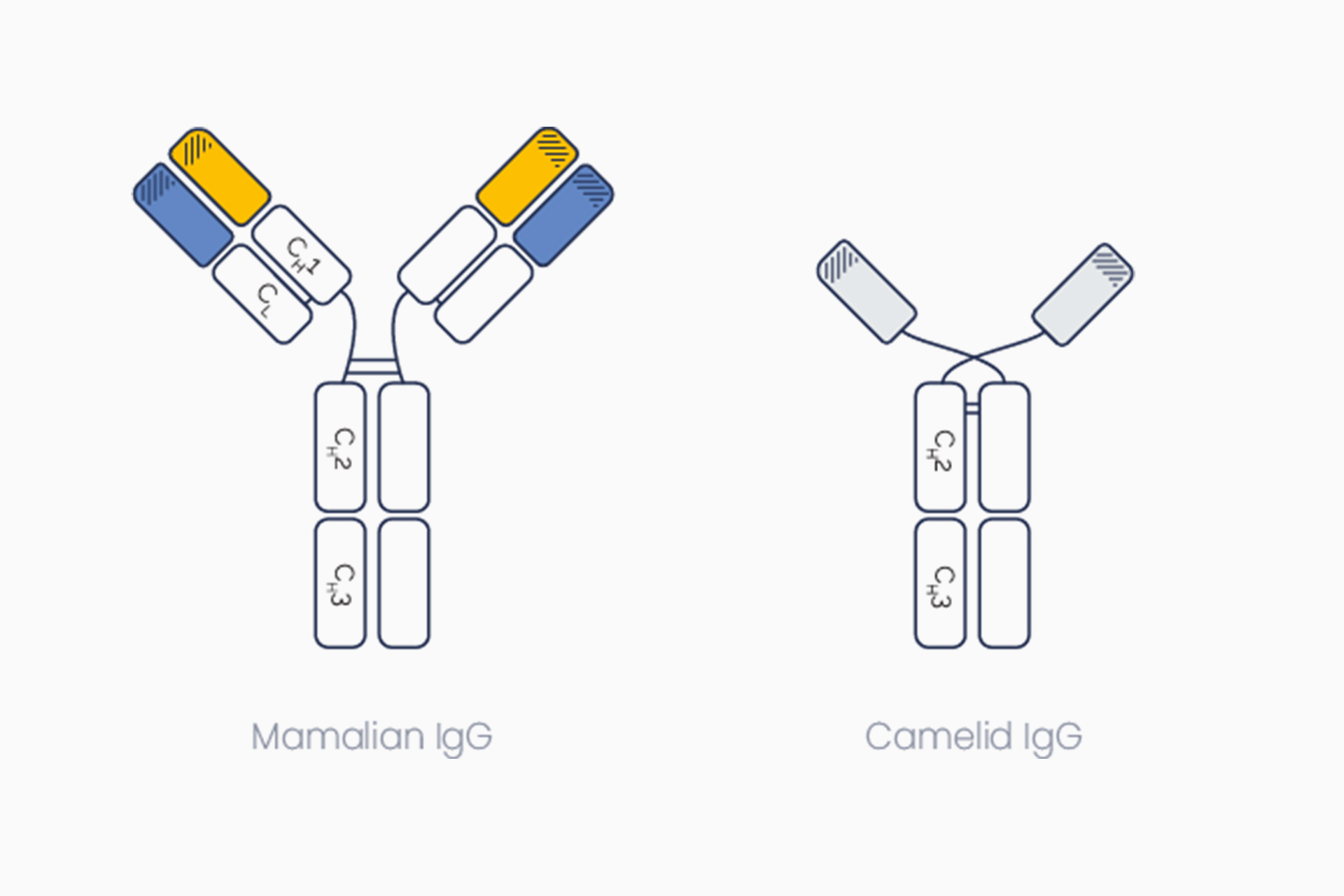
Сравнение обычных антител млекопитающих (слева) и нано-антител ламы (справа)
Над новыми вакцинами от ВИЧ трудились и в России. В 2015 году одна из них, «ДНК-4», после 18 лет работы дошла до второй фазы клинических испытаний. По словам руководителя научной группы Алексея Козлова, ее развитие позже свернули, что он назвал «следствием непонимания проблемы». Однако большинство вакцин от ВИЧ вообще не доходило до тестирования на людях из-за низкой эффективности или других проблем. Некоторые терпели неудачу уже на финишной прямой. Такая история случилась и с американской вакциной Uhambo, которую объявили неэффективной на третьей фазе клинических испытаний. В итоге инвесторы после многих лет ожидания потеряли 104 миллиона долларов.
Еще одну отечественную вакцину — на основе нано-антител ламы — в прошлом году начали испытывать на мышах в Новосибирске. Такая вакцина активирует B-клетки человека. Эти клетки обеспечивают гуморальный иммунный ответ — вырабатывают антитела против инфекции. Для создания препарата антитела лам (как и других представителей семейства верблюдовых) подходят лучше человеческих, так как отличаются маленьким размером и более простой структурой. Поэтому их гораздо проще синтезировать в лаборатории и видоизменять для производства вакцин от новых патогенов, чем человеческие антитела. Из-за своей более простой структуры нано-антитела ламы также более стабильны, а значит, лучше подходят для хранения и транспортировки.
Но, даже если вакцина, которая может предотвратить ВИЧ, появится прямо сейчас, в мире все еще останется около 40,1 миллиона зараженных. Поэтому разработка лекарств всегда будет приоритетом. Тем более если мы хотим покончить с ВИЧ-эпидемией к 2030 году, к чему стремится Всемирная организация здравоохранения.
Автор: Екатерина Мищенко